الفرق بين العدد الذري والعدد الكتلي
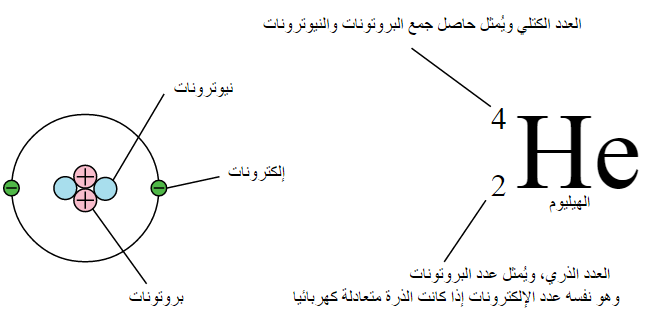
العدد الذري والعدد الكتلي من أهم المفاهيم المستخدمة والمتعلقة بنواة ذرة أي عنصر موجود، وحيث أن الذرة الواحدة تحوي ما هو أصغر منها من النيترونات المتعادلة، والبروتونات الموجبة، والإلكترونات السالبة حول نواة الذرة، لابد من وضع تعريفات محددة خاصة بكل جسيم منهم.
ما هو العدد الكتلي

يمكننا إجمال ما يخص العدد الكتلي للعناصر والذرات الكيميائية فيما يلي:
العدد الكتلي هو مصطلح يعبر بصورة أساسية عن أعداد النيترونات، والبروتونات بداخل نواة ذرة العنصر، ويعبر حاصل جمعهما معا عن العدد، أو الوزن الكتلي لذرة عنصر معين ويكون هذا الرقم في صورة وحدة صحيحة مجردة لأنها تعبر فقط عن أعداد.
إذا تشابهت أعداد العناصر الذرية فمن المستحيل أن تتشابه في أعدادها الكتلي، وعندما تكون مجموعة عناصر متشابهة في أعدادها الذرية فقط دون الوزن الكتلي لها، يعرف هذا بالنظائر للعنصر الواحد.
يتواجد العدد الكتلي كرقم مكتوب بخط صغير، وواضح في أعلى يسار العنصر، ومن الوارد أن يكتب بجانبه ولا يتم استخدام كلا من العدد الذري، والعدد الكتلي معا إلا في حالات دراسة انشطارات النواة لملاحظة الاختلاف الحادث في النيترونان، والبروتونات.
من المنطقي والبديهي أن ندرك أنه كلما زادت الكتلة الذرية للعنصر كلما زاد وزنه وجعله هذا أثقل بكثير عن الطبيعي فتقوم النواة بالانشطار،
لتقليل كمية الطاقة بداخلها، بينما إذا كان الوزن الكتلي لها صغير أي تصبح أخف من الطبيعي، يجعلها هذا تميل إلى الاندماج مع نواة عنصر آخر للوصول لحالة الاتزان الكيميائي والاستقرار.
تعرف على: بحث شامل عن العناصر والمركبات
ما هو العدد الذري
العدد الذري هو العدد الذي يعبر وبالتحديد عن عدد البروتونات الموجبة في نواة الذرة الواحدة، أي أنه يمكن للشخص معرفة عدد البروتونات التي تحتويها نواة الذرة، عند قراءة العدد الذري للعنصر، فعلى سبيل المثال: –
تحتوي ذرات الهيدروجين على بروتون واحد فقط، أي أن العدد الذري لعنصر الهيدروجين هو 1، تحتوي ذرات الهيليوم على 2 بروتون،
لذلك فالعدد الذري لعنصر الهليوم هو2، والعدد الذري مقدار ثابت، لا يتغير أبدًا، ويعني ذلك أن عدد البروتونات في نواة كل ذرة داخل عنصر معين، هو عدد ثابت أيضًا.
تكمن أهمية العدد الذري في أنه السبب الرئيسي في أنه يمكن للشخص أن يقوم بتحديد عنصر الذرة من خلاله، وللعدد الذري أيضًا دور أساسي ومهم في تحديد خصائص العناصر.
كما أنه يوجد أهمية أخرى للعدد الذري، هو أن الجدول الدوري للعناصر الكيميائية، الذي يتم اتباعه في الوقت الحالي من قبل المؤسسات العلمية وغيرها، قائم ومنظم وفقاً للعدد الذري تصاعدياً من اليسار إلى اليمين.
قد يحدث وتتشابه العناصر مع بعضها في أعدادها الذرية، ولكن تختلف فقط في عددها الكتلي، وهو المتعارف عليه دوليًا باسم النظائر، وبالتالي يكون هذا الاختلاف راجع إلى زيادة، أو نقص أعداد النيترونات في نواة ذرات هذه العناصر.
لا يفوتك معرفة: بحث عن العوامل المؤثرة في سرعة التفاعل الكيميائي
الفرق بين العدد الذري والعدد الكتلي

لابد أن نأخذ في الاعتبار أن هناك تلامس كبير بين كلاهما حيث أن:
الفرق بين العدد الذري والعدد الكتلي يكون فقط في تعريفهما، حيث أن العدد الذري هو عدد البروتونات الموجبة في نواة ذرة العنصر،
ويرمز له بالحرف الإنجليزي”Z “. بينما العدد الكتلي هو في كيمياء الذرة، مجموع قيمة البروتونات الموجبة والنيوترونات المتعادلة الشحنة، ويرمز له بالرمز”A “.
عن طريق معادلة حساب العدد الكتلي نستنتج أن كتلة الذرّة تلخص وتختصر في نواتها المكونة من البروتونات والنيوترونات فقط، حيث يتم تجاهل الكتلة الصغيرة للإلكترونات السالبة والتي تدور حول نواة العنصر في حساب العدد الكتلي.
يساعد العدد الذري في التنبؤ وتحديد الخصائص الكيميائية والفيزيائية للذرة، بينما تكمن أهمية العدد الكتلي في تحديد درجة ثبات العناصر، وما يحدث بها من اختلافات من حيث أعداد البروتونات، والنيترونات أثناء تفاعلاتها.
العدد الكتلي يساوي
يمكن حساب العدد الكتلي لأي عنصر من خلال المعادلة الرياضية الآتية:
- العدد الكتلي= عدد البروتونات + عدد النيوترونات
حيث أن كتلة الإلكترونات لا تدخل في حساب العدد الكتلي؛ نظرًا لكتلتها الصغيرة جدًا، كما يمكن معرفة عدد النيوترونات من خلال طرح العدد الذري من العدد الكتلي بمعنى أن
- عدد النيوترونات= العدد الكتلي – العدد الذري.
قد يهمك أيضًا: ما هي مصادر العناصر المشعة
قانون العدد الذري
- هو عبارة عن عدد البروتونات الموجودة في نوية ذرة العنصر، وبما أنه ذرات العناصر المختلفة متعادلة كهربياً فهذا يعني أن عدد البروتونات = عدد الإلكترونات.
- لذلك يمكن القول: العدد الذري =عدد البروتونات الموجبة= عدد الإلكترونات السالبة، والتي تدور حول النواة.
شاهد أيضًا: معلومات تفصيلية عن العناصر الخاملة
ما هو عدد النيترونات؟
- العدد الذريّ=عدد البروتونات= عدد الإلكترونات.
- العدد الكتليّ=عدد البروتونات+ عدد النّيوترونات.
وبما أن كلاً من العدد الذريّ والعدد الكتليّ للعنصر معروفان، فإنه من السهل جدًا علينا أن نعرف عدد النّيوترونات، وذلك باستخدام هذه المعادلة: عدد النّيوترونات=العدد الكتليّ – عدد البروتونات.
حساب العدد الكتلي
من السهل جدًا علينا حساب العدد الكتلي، أو الوزن الكتلي لأي عنصر من خلال معرفة كل من عدد البروتونات، والنيترونات، وذلك من خلال القانون التالي:
- العدد الكتلي= عدد البروتونات الموجبة+ عدد النيترونات المتعادلة داخل نواة الذرة.
ننصحك بقراءة: اسماء عناصر الجدول الدوري بالعربي
في خلاصة الموضوع نستطيع اعتبار أن الأعداد الذرية صفة مميزة وفريدة لكل عنصر من عناصر الجدول الدوري، لأنه ببساطة إن حدث اختلاف في عدده الذري سيؤدي إلى اختلاف في عدده الكتلي، وبالتالي اختلال في تركيبه وبالتالي نوعه كعنصر.









